EXERCÍCIOS BÁSICOS DE QUÍMICA I
NOX
O número de oxidação informa o
número de elétrons que um átomo ou íons doou ou recebeu quando unido com outro
átomo ou íon.
TABELA DE NOX FIXO
Família 1: +1
Família 2: +2
Alumínio: +3
Zn: +2
Ag: +1
Halogênios com apenas um outro
elemento: -1, ex: cloro, iodo, bromo.
Hidrogênio: geralmente +1; quando
com outro elemento da família 1 então -1
Oxigênio: geralmente -2, em
peróxidos -1.
Enxofre: com apenas um outro
elemento -2 (não pode ser o oxigênio)
Quando o elemento for simples (O2,
H2, ...) o NOX é zero.
O nox da hidroxila (OH) é -1
O resto dos elementos devemos
calcular o NOX
Ex:
NaCℓ = como o sódio é da família
1, o seu nox é +1, e como o cloro é halogênio e está ligado a apenas um outro
elemento, o seu nox é -1.
PbO2, primeiro devemos
tentar descobrir o nox de cada um. O Pb é da família 14, então não apresenta
nox fixo (que pena), mas o oxigênio tem nox -2.
Para montar o cálculo devemos ver
se a molécula tem alguma carga sobre ela na esquerda
Como não apresenta, vamos igualar
a zero e colocar o nox de quem já sabemos, o oxigênio.
Depois devemos multiplicar o nox
pelo número de oxigênios.
Depois devemos descobrir o número
que somado com -4 para zerar, que deve ser o +4
Agora é só subir dividindo pelo
número de chumbo (1), que não aparece abaixo do chumbo.
H2SO4 =
primeiro devemos saber o nox dos elementos das pontas, o O = -2, e o H = +1.
Depois montamos o tabela para
descobrir o nox do elemento central, se a substância não for um ácido, devemos saber dois NOX, não interessando a posição do elemento.
Agora desce multiplicando o nox
do oxigênio e o nox do hidrogênio pelo número de oxigênios e hidrogênios.
Agora devemos ver o número que
somado com o dois e subtraído do 8 resulta em zero (+ 6), então subidos ele
dividindo pelo número de enxofre, que é um, o que resulta em + 6 o nox do
enxofre.
Quando a substância já apresentar
uma carga, negativa ou positiva, devemos colocar está carga no lugar do zero do
resultado, como por exemplo:
Vamos descer a carga para o lugar
do zero.
Agora é ver o nox de quem já
sabemos, no caso o hidrogênio = +1 e multiplicar pelo número de hidrogênios
(4), que resulta em uma carga +4.
Agora devemos ver o valor que
somado com +4 resulta em + 1, logo é o -3, que será a carga do nitrogênio.
Então para descobrir o nox do
nitrogênio devemos dividir a carga dele pelo número de nitrogênios (1), o que
resulta em um nox -3.
Vamos fazer os exercícios de
fixação para melhorar os conhecimentos de como descobrir o nox dos elementos.
1. Calcule
o nox dos elementos abaixo.
a)
CO2
b)
CO
c)
C6H12O6
d)
H3PO4
e)
H3PO3
f)
HPO3
-2
g)
HCℓO
h)
HCℓO2
i)
HCℓO3
j)
HCℓO4
k)
H2SO4
l)
H2SO3
m)
SO2
n)
SO3
o)
H2S
p)
PbO
q)
PbO2
Alguns íons tem o seu nox fixo, o
que é bom saber em alguns casos
SO4 = -2
CO3 = -2
NO2 = -1
CℓO4 = -1
PO4 = -3










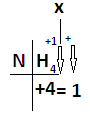


Nenhum comentário:
Postar um comentário